Endoskopisk ultralyd (EUS) har etablert seg som et helt sentralt ledd i diagnostikk og behandlingsstrategi ved pankreaskreft. Gjennom EUS-veiledet finnålsaspirasjon (FNA) eller biopsi (FNB) kan man sikre histologisk diagnose med høy presisjon, samtidig som metoden åpner for skreddersydd og målrettet kreftbehandling.
En nylig populasjonsbasert prospektiv studie fra Oslo universitetssykehus, Rikshospitalet – NORPACT-2 – har undersøkt ytelse og sikkerhet ved EUS-FNA/FNB og ERCP hos pasienter med borderline resektabel (BRPC) og lokalavansert pankreaskreft (LAPC). Studien representerer en større systematisk gjennomgang av disse prosedyrene i en prospektiv, uselektert, regional pasient kohort.
Behov for rask og presis vevsdiagnose
Pankreaskreft forventes å bli den nest hyppigste årsaken til kreftrelatert død innen 2030 (1). Flertallet av pasientene presenterer dessverre med metastatisk sykdom på diagnosetidspunktet (50 %), mens kun 15 % er kan opereres direkte. 35 % av pasientene presenterer med borderline-resektabel (BRPC) eller lokalavansert (LAPC) sykdom der tumor affiserer sentrale blodkar i varierende grad og dermed ikke ansees som direkte teknisk resektabel.
Kirurgi er eneste kurative behandling. For pasienter uten fjernmetastaser, men med BRPC eller LAPC, er neoadjuvant kjemoterapi anbefalt som førstelinjebehandling (2). Formålet med neoadjuvant kjemoterapi er å øke andel av frie reseksjonsrender (R0) samt å redusere størrelsen på tumor slik at den kan bli teknisk resektabel. Tumorskrumpning fasiliterer for at flere pasienter kan gjennomgå kurativ kirurgisk reseksjon.
For å kunne starte neoadjuvant behandling kreves sikker histologisk bekreftelse av malignitet og effektiv avlastning ved eventuell obstruktiv ikterus. EUS benyttes for vevsprøvetaking, mens endoskopisk retrograd cholangiopankreatografi (ERCP) er standard for biliær stenting (3).
Studiepopulasjon og metode
I perioden 2018–2020 ble 251 pasienter med radiologisk BRPC eller LAPC inkludert. 230 av disse gjennomførte endoskopisk utredning.
- 223 (89 %) gjennomgikk EUS-FNA/FNB for vevsdiagnose. (Tabell 1)
- 133 (53 %) fikk utført ERCP med stentinnleggelse.
- 41 pasienter hadde kombinert EUS og ERCP i samme seanse.
De fleste undersøkelsene ble utført ved Rikshospitalet av erfarne endoskopører. Rapid On-Site Evaluation (ROSE) ble brukt der det var tilgjengelig, slik at man ved usikkerhet kunne ta ny prøve under samme endoskopiseanse.
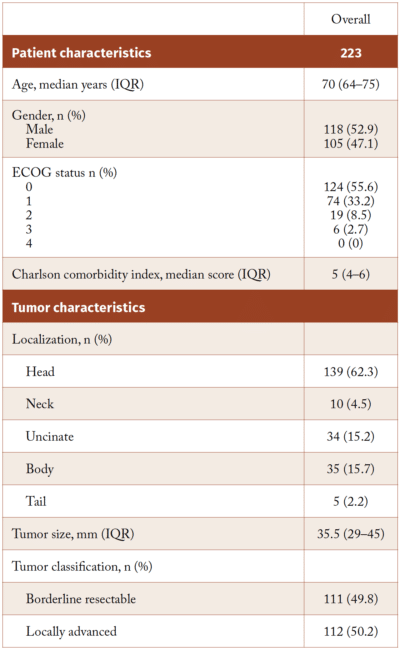
Table 1. Pasient karakteristika for 223 pasienter som gjennomgikk EUS FNA/FNB. (Farnes I et al. Scand J Gastroenterol. 2024 Apr;59(4):496-502.)
Resultater: Høy diagnostisk presisjon og lav risiko
EUS-FNA/FNB viste meget god ytelse:
- Diagnostisk nøyaktighet ved første forsøk: 86 %.
- Kumulativ nøyaktighet etter gjentatte forsøk: 96 %.
- Falsk positiv malignitet: kun 0,9 %.
Hos ca. 15 % av pasientene var det behov for gjentatt EUS, som i nesten alle tilfeller førte til korrekt diagnose. (Figur 1) Kombinasjon av FNA og FNB ble brukt i 83 prosedyrer, og bidro til økt vevskvalitet for immunhistokjemiske og molekylære analyser – i tråd med nyere anbefalinger om EUS-FNB som førstevalg ved avansert sykdom (4).
For ERCP var suksessraten 80 % ved første forsøk og 94 % etter to forsøk. Flertallet fikk innlagt selv-ekspanderende metallstent (SEMS), som har lengre levetid og lavere reintervensjonsrate enn plaststenter (5). Dette er spesielt viktig ettersom flertallet av pasientene mottar neoadjuvant kjemoterapi over flere måneder og et stentbytte vil kunne resultere i uønskete komplikasjoner og forsinkelser i behandlingen.
Kombinert EUS og ERCP i én seanse viste seg både praktisk og trygt, i tråd med internasjonale retningslinjer, samtidig som det er en tidsbesparende strategi når det er praktisk mulig (6).
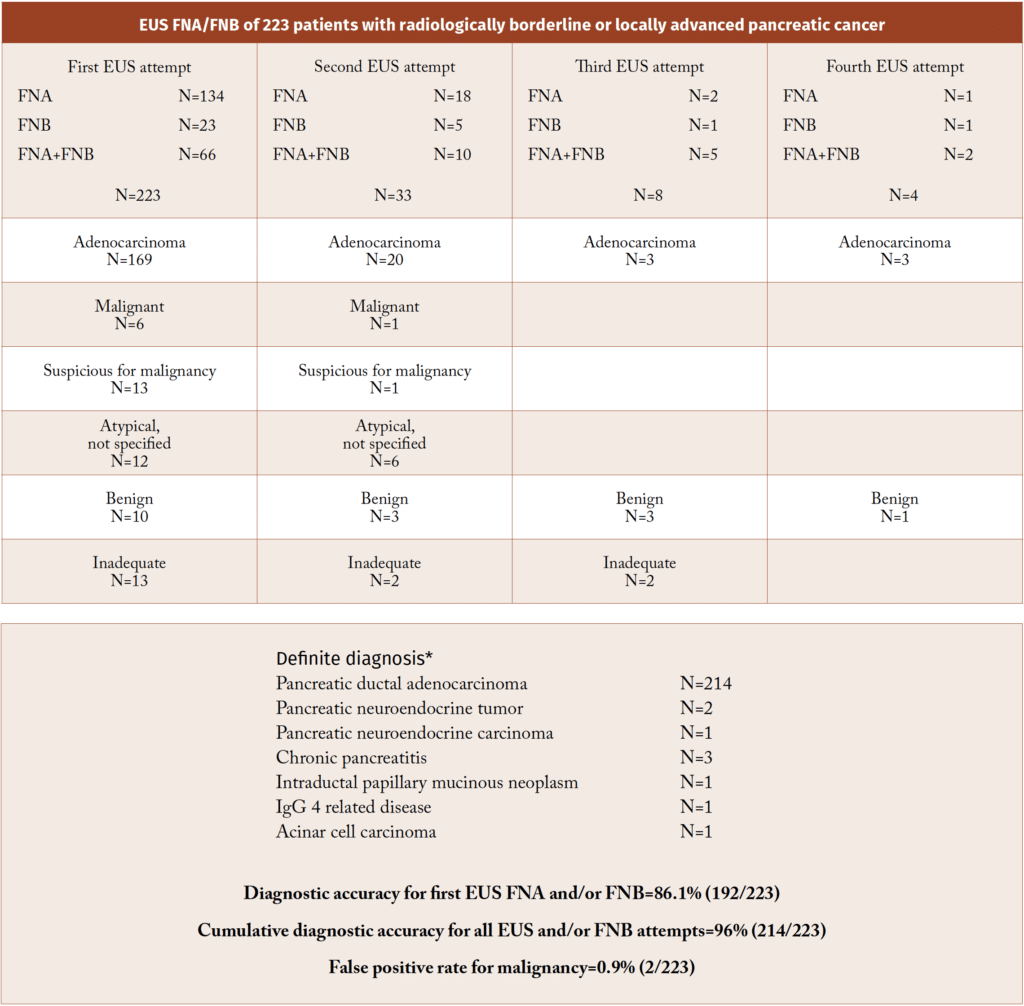
Figur 1: Patologisk resultat av cytologi/biopsi etter 268 EUS FNA/FNB hos 223 pasienter med radiologisk diagnose BRPC eller LAPC. ( Farnes I et al. Scand J Gastroenterol. 2024 Apr;59(4):496-502.)
Komplikasjoner
Komplikasjonsfrekvensen i vår kohort var lav (Tabell 2):
- EUS-FNA/FNB: 3 % (primært pankreatitt).
- ERCP: 15 % (primært pankreatitt, kolangitt).
- Kombinert EUS + ERCP: 10 %.
De fleste hendelser var milde og forbigående, og alvorlige komplikasjoner var sjeldne (< 1 %). Disse tallene samsvarer godt med internasjonal litteratur (7).
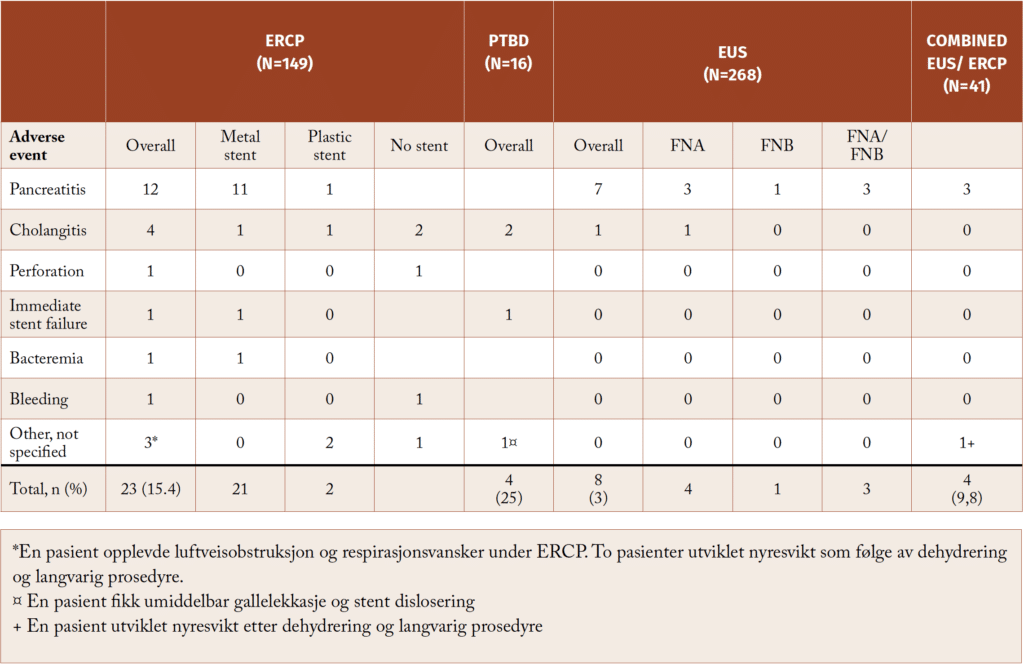
Table 2: Prosedyrerelaterte komplikasjoner etter ERCP, PTC/PTBD eller EUS FNA/FNB (Farnes I et al. Scand J Gastroenterol. 2024 Apr;59(4):496-502.)
Klinisk betydning
Studien viser at EUS-basert vevsprøvetaking er både sikker og svært presis, og at gjentatt EUS ved ikke-konklusiv første prøve gir høy gevinst. Metoden gir tilstrekkelig materiale ikke bare for histologi, men også for molekylærpatologisk analysering. Dette er særlig relevant ettersom internasjonale retningslinjer (NCCN, ESMO) nå anbefaler EUS-FNB ved BRPC og LAPC for å muliggjøre målrettet og persontilpasset kreftbehandling (8). Testing for MSI og KRAS er nå implementert i nasjonalt handlingsprogram for pancreascancer.
Resultatene understøtter også at kombinert diagnostisk og terapeutisk EUS-/ERCP-seanse er trygg, og kan bidra til raskere oppstart av neoadjuvant behandling – et sentralt mål i et behandlingsforløp hvor tid til terapi er avgjørende for prognose.
Konklusjon
Denne norske, populasjonsbaserte studien dokumenterer at:
- EUS-FNA/FNB gir 96 % diagnostisk treffsikkerhet og lav komplikasjonsrate.
- ERCP lykkes i over 80 % av tilfellene ved første forsøk, og nær 94 % totalt.
- Samtidig EUS og ERCP kan trygt utføres og effektivisere pasientforløpet.
EUS-veiledet vevsprøvetaking fremstår dermed som hjørnesteinen i diagnostikk og behandlingsplanlegging ved BRPC og LAPC, og utgjør et avgjørende grunnlag for fremtidens målrettede, presisjonsbaserte pankreaskreftbehandling.
Kilder:
- Rahib L, Smith BD, Aizenberg R, et al. Projecting cancer incidence and deaths to 2030: the unexpected burden of thyroid, liver, and pancreas cancers in the United States. Cancer Res. 2014;74(11):2913– 2921. doi: 10.1158/0008-5472.CAN-14-0155
- Tempero MA, Malafa MP, Al-Hawary M, et al. Pancreatic adenocarcinoma, version 2.2021, NCCN clinical practice guidelines in oncology. J Natl Compr Canc Netw. 2021;19(4):439–457. doi: 10.6004/ jnccn.2021.0017.
- Dumonceau JM, Deprez PH, Jenssen C, et al. Indications, results, and clinical impact of endoscopic ultrasound (EUS)-guided sampling in gastroenterology: European society of gastrointestinal endoscopy (ESGE) clinical guideline – updated january 2017. Endoscopy. 2017;49(7):695–714. doi: 10.1055/s-0043-109021.
- Levine I, Trindade AJ. Endoscopic ultrasound fine needle aspiration vs fine needle biopsy for pancreatic masses, subepithelial lesions, and lymph nodes. World J Gastroenterol. 2021;27(26):4194–4207. doi: 10.3748/ wjg.v27.i26.4194.
- Almadi MA, Barkun A, Martel M. Plastic vs. self-expandable metal stents for palliation in malignant biliary obstruction: a series of meta-analyses. Am J Gastroenterol. 2017;112(2):260–273. doi: 10.1038/ ajg.2016.512. stents for palliation in malignant billary obstruction: a series of meta-analyses. Am J Gastroenterol. 2017;112(2):260-273. doi: TO. 1038/ ajg.2016.512.
- Jenssen C, Hocke M, Fusaroli P, et al. EFSUMB guidelines on interventional ultrasound (INVUS), part IV – EUS-guided interventions: general aspects and EUS-guided sampling (long version). Ultraschall Med. 2016;37(2):E33– E76. doi: 10.1055/s-0035-1553785.
- Cotton PB, Eisen GM, Aabakken L, et al. A lexicon for endoscopic adverse events: report of an ASGE workshop. Gastrointest Endosc. 2010;71(3):446– 454. doi: 10.1016/j.gie.2009.10.027.
- Mosele F, Remon J, Mateo J, et al. Recommendations for the use of next-generation sequencing (NGS) for patients with metastatic cancers: a report from the ESMO precision medicine working group. Ann Oncol. 2020;31(11):1491–1505. doi: 10.1016/j.annonc.2020.07.014.