Av Jon Arne Søreide, Seksjonsoverlege/professor, Avd. for gastroenterologisk kirurgi, Stavanger universitetssjukehus. [email protected]
Av Jon Arne Søreide, Seksjonsoverlege/professor, Avd. for gastroenterologisk kirurgi, Stavanger universitetssjukehus. [email protected]
Nasjonalt handlingsprogram med retningslinjer for diagnostikk, behandling og oppfølging av pasienter med pancreaskreft er helt nytt og ble publisert på Heldirektoratets hjemmesider i januar 2014 (http://helsedirektoratet.no/publikasjoner/). Dette dokumentet omfatter også utredning og behandling av cystiske pancreaslesjoner.
PANCREASKREFT
Forekomst
Årlig blir over 600 nye pasienter diagnostisert med pancreaskreft i Norge, som tilsvarer en samlet insidens på 14/100 000/år. Forekomsten er tilnærmet lik for begge kjønn og øker betydelig med alder over 60 år. På diagnosetidspunktet har mange pasienter enten metastatisk eller lokalavansert sykdom, og noen har tilleggssykdommer som gjør at operativ behandling ikke er mulig. Dermed kan kun 15-20 prosent av pasientene bli tilbudt operativ behandling med kurativ intensjon. Selv hos de som blir ”radikalt” operert er 5-årsoverlevelsen lav.
Diagnostikk
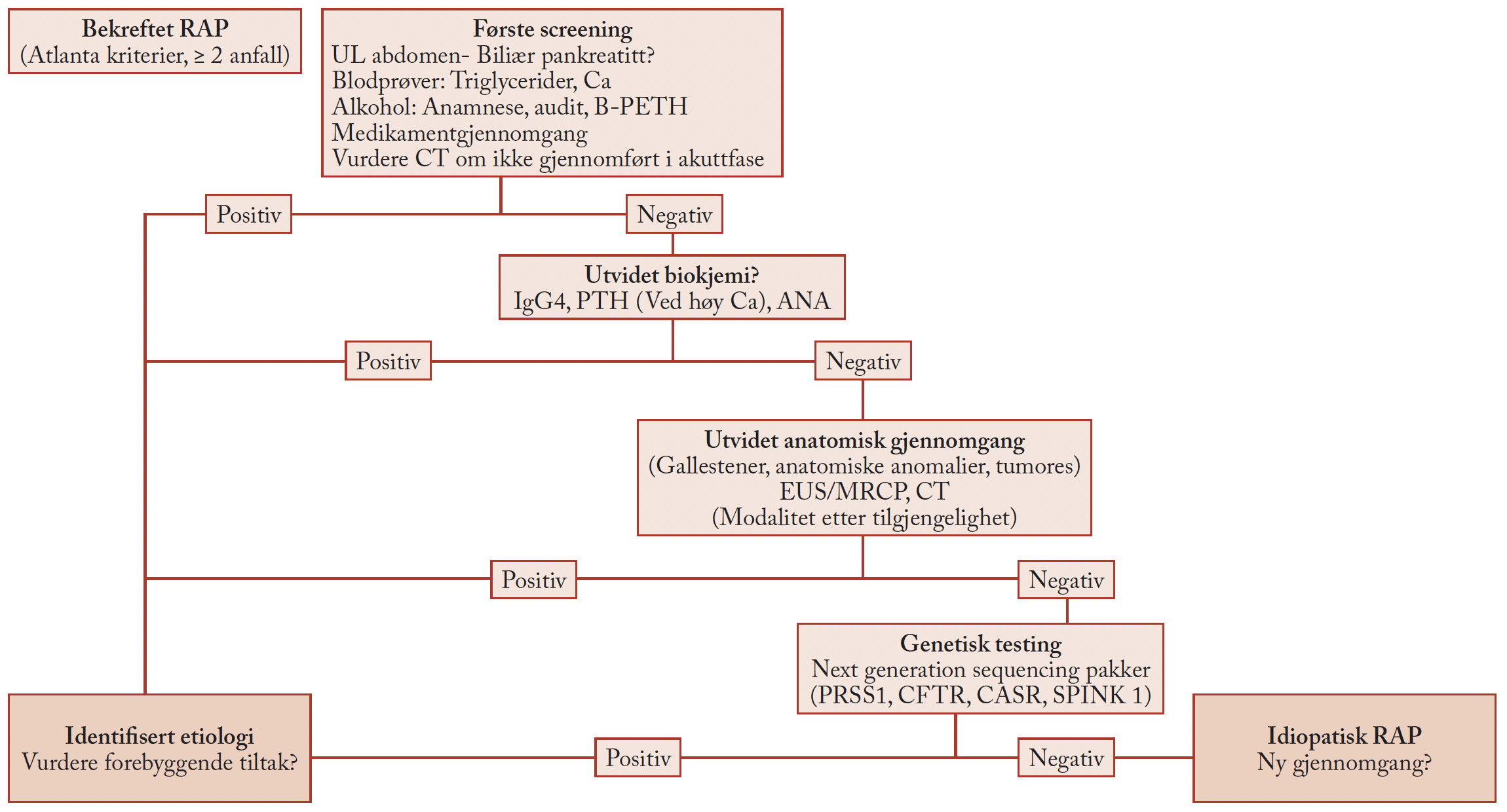
Tidlig diagnostikk er viktig, men ofte vanskelig. Kliniske symptomer er vage og uspesifikke. Ikterus og ufrivillig vekttap, eventuelt i kombinasjon med smerter, er alarmtegn. Nyoppdaget diabetes mellitus hos en pasient uten kjente risikofaktorer bør også lede til videre utredning.
Adekvat bildediagnostikk, ofte med computer diagnostikk (CT) i portovenøs fase, bør rekvireres ved mistanke om alvorlig abdominal sykdom. For spesifikk tumordiagnostikk i pancreas, gjøres CT med pancreasprotokoll, som inkluderer 2-fase kontrast-undersøkelse, der man også tar med abdomen/bekken og thorax. Vurdering av resektabilitet baserer seg på adekvat bildediagnostikk, og endelig utredning/vurdering bør utføres der hvor pasienten eventuelt skal opereres (Figur 1). Både MR og EUS kan være supplerende modaliteter i enkelte tilfeller. ERCP har liten plass i diagnostisk sammenheng, men er en aktuell prosedyre ved for eksempel galleavlastning. Det er svært viktig at optimal bildediagnostikk blir utført før man avlaster galleveiene med stent.
Tumormarkører (forhøyet CA 19-9 ved ductal adenocarcinom eller kolangiocarcinom eller forhøyet CgA ved nevroendokrin tumor) kan gi en viss støtte i tumorutredningen, på samme måte som forhøyet IgG4 kan gi en viss diagnostisk støtte ved klinisk mistanke om autoimmun fokal pancreatitt.
En best mulig utredning basert på adekvat bildediagnostikk og noen ganger supplert med for eksempel EUS er viktig for adekvat utredning av både solide og cystiske pancreaslesjoner.
Behandling
Kirurgi er den aller viktigste terapeutiske modalitet hos pasienter som vurderes for behandling med kurativ intensjon. Pasienter med tumor lokalisert til caput pancreatis/periampullært blir vurdert for pancreatoduodenektomi (gjerne kalt ”Whipples operasjon”), ofte i en pylorusbevarende modifikasjon (Figur 2). Distale reseksjoner med splenektomi blir gjort om tumor er lokalisert i cauda eller corpus pancreatis. Hvis det er liten mistanke om at pancreaslesjonen er malign, vil man gjerne tilstrebe en miltbevarende distal reseksjon. Total pancreatectomi utføres svært sjelden, og da gjerne hos pasienter som har fått påvist intraductal papillær mucinøs neoplasi (IPMN) med påvist eller mistanke om affeksjon av hele hovedgangen i pancreas.
Pancreasreseksjoner er krevende operasjoner. Denne type kirurgi blir nå i all hovedsak utført ved 5 universitetssykehus ( OUS-Oslo, SUS-Stavanger, HUS-Bergen, St.Olav-Trondheim, og UNN-Tromsø). Likeså viktig som selve den kirurgiske kompetansen er en døgnkontinuerlig kompetanse og kapasitet hos andre involverte avdelinger: anestesi-/intensivavdeling, radiologisk avdeling med invasive prosedyrer, endoskopilaboratorium. Avdeling for patologi og onkologisk avdeling er avgjørende for det samlede behandlingstilbudet.
Adjuvant kjemoterapi er nå et standardtilbud for alle (< 75 år) som er operert for adenocarcinom i pancreas, uavhengig av lymfeknutemetastaser eller ikke. Enten 5-FU/leucoverin- eller gemcitabin-basert adjuvant behandling bør påbegynnes innen 8 uker etter operasjonstidspunktet, og behandlingen varer i 6 mnd.
Oppfølging etter kurativ behandling
Postoperativ kontroll hos kirurg 4-6 uker etter operasjonen er viktig for å formidle ny informasjon (inkludert endelig histologibeskrivelse), og for å imøtekomme det informasjonsbehovet pasienten og pårørende måtte ha. Dessuten er det viktig å vurdere pasientens allmenn- og ernæringstilstand, ikke minst med tanke på å kunne starte på adjuvant kjemoterapi.
Under pågående kjemoterapi blir pasienten fulgt av onkolog. Etter avsluttet primærbehandling vil pasienten som en hovedregel bli fulgt videre av sin fastlege. Det er ikke vitenskapelig støtte for å si at tett oppfølgning ved sykehus-poliklinikk, og/eller standardisert rutinemessig bildediagnostikk bedrer prognosen for denne pasientgruppen. Om nye kliniske problemstillinger dukker opp i forløpet, må fastlegen henvise pasienten til relevant bildediagnostikk og/eller til utredning og vurdering ved aktuell spesialistpoliklinikk.
Palliativ behandling av inoperabel tumor eller metastaserende kreftsykdom
De fleste pasienter med pankreas-kreft har allerede på diagnosetidspunktet avansert sykdom som ikke er tilgjengelig for kurativ behandling. Selv hos de som blir operert med kurativ intensjon, vil svært mange få sykdomstilbakefall. Vanligst er metastaser til lunge, lever, lymfeknuter eller peritoneum, med eller uten lokalt residiv. Hos pasienter med lokalavansert sykdom (uten metastaser) er median overlevelse mellom 9-12 måneder, den mediane overlevelsen er redusert til mellom 3-6 måneder om det er påvist metastaser.
Om pasienten har en adekvat funksjonsstatus (ECOG≤1-2) kan systemisk palliativ kjemoterapi vurderes. Behandling med gemcitabin har gitt økt overlevelse sammenlignet med 5-FU-basert behandling. Nyere data tyder på at FOLFIRINOX kan bedre overlevelsen ytterligere, men med en noe høyere bivirkningsprofil. Andre medikamenter og regimer er på vei inn i klinisk anvendelse.
Denne pasientgruppen vil ofte ha behov for palliative tiltak både for å avlaste obstruksjoner (endoskopisk avlastning av f.eks. galleveier eller duodenum med SEMS, eller ventrikkelen med en PEG), men også
lindre smerter (adekvat smertebehandling medikamentelt, men i tillegg for eksempel CT- eller EUS-veiledet cøliakusblokade). Generelle palliative tiltak og nyttig informasjon er godt beskrevet i eget Handlingprogram for palliasjon i kreftomsorgen (se Helsedirektoratets hjemmeside).
CYSTISKE PANCREASLESJONER
Utredning og behandling av cystiske pancreaslesjoner er en voksende del av virksomheten innen gastroenterologien. Disse lesjonene er ofte et tilfeldig funn ved utredning av symptomer eller tilstander som ikke er relatert til pancreas. Økende bruk av bildediagnostikk, ikke minst i primærhelsetjenesten, avdekker lesjoner som i neste omgang henvises til spesialistpoliklinikk for videre avklaring, og eventuelt behandling eller råd om oppfølgning.
I hovedsak kan vi dele de cystiske lesjonene i to hovedgrupper:
1. Lesjoner uten malignitetspotensiale
a. Pseudocyste (pancreatitt i sykehistorien – avventende til invasiv behandling)
b. Serøse cystadenomer (”serøs cystisk neoplasi”; vanligvis hos kvinner>60-70 år, ”aldri” maligne, oftest multicystiske bikubemønster, sentralt arr med kalk – sjelden indikasjon for operasjon)
2. Lesjoner med malignitetspotensiale
a. Mucinøse adenomer (”mucinøs cystisk neoplasi”; nesten alltid lokalisert til cauda/corpus , oftest kvinner ≈ 40-50-års alder. Ingen kommunikasjon med pancreasgangs-ystemet. Indikasjon for kirurgi.)
b. Intraductal mucinøs cystisk neoplasi (IPMN)
i. Hovedgangs- IPMN (Høy risiko for malignitet hvis diameter≥ 10 mm og kontrastoppladende murale knuter. I operasjonsmaterialer er inntil 2/3 maligne, og vel 40 % invasive. Indikasjon for kirurgi.)
ii. Sidegangs-IPMN definert som pancreascyster >5 mm som kommuniserer med pancreas-hovedgangen. Malignitetsrisiko vurderes bl.a. relatert til diameter på lesjon, men individuell vurdering er nødvendig.
c. Solid pseudopapillær neoplasi(SPPN)
i. Også kalt ”Franz-tumor”; yngre kvinner omkring 20-30 år, langsomtvoksende.
ii. Ofte stor tumor ved diagnose – radikal operasjon gir god prognose.
I handlingsprogrammet gis noen retningslinjer for hvilke pasienter som bør følges opp, og på hvilken måte. Disse er veiledende og bør tilpasses individuelt. Vurdering av hver enkelt pasient (alder, komorbiditet, lesjonens størrelsen og karakteristika, vekst over tid – og ikke minst pasientens ønske om behandling, eller evne/vilje til å leve med en liten diagnostisk usikkerhet) er nødvendig der det ikke er åpenbar indikasjon for operativ behandling.
Følgende har deltatt i gruppen som har laget handlingsprogrammet:
Anders Drolsum, Svein Dueland, Tor Jacob Eide, Ivar P. Gladhaug, Jon Erik Grønbech, Marianne Klemp, Kristoffer Lassen, Marit Olstad, Åse Skår, Rune Småland og Jon Arne Søreide (leder)