Av Georg Dimcevski & Odd Helge Gilja. Nasjonalt Senter for Gastroenterologisk Ultrasonografi (NSGU) og Gastroenterologisk seksjon, Medisinsk avdeling, Haukeland Universitetssykehus, Bergen,Klinisk institutt 1, Universitetet i Bergen, Bergen.
Ultralydavbildning er en trygg, billig, pålitelig og en av de mest populære diagnostiske teknikker. I klinisk ultralyd, kan blodlegemer ikke differensieres fra det omkringliggende vev, på grunn av lav akustisk impedansforskjell mellom blodlegemer og deres omgivelser.
Tilsettelse av biokompatible kontrastmidler i blodet bidrar til å skille mellom blod og andre typer vev. Slike ultralydkontrastmidler består av lavoppløselig gass, dvs. gassbobler som er innkapslet i et stabiliserende skall. Med gjennomsnittlig diameter under 6 mikroner, er disse mikroboblene små nok til å passere gjennom lungekapillærene. Det har blitt påvist av mange forskergrupper at cellulært opptak av medikamenter og gener økes når regionen/organet av interesse er i et ultralydfelt. Denne effekt kan forsterkes enda mer når et ultralydkontrastmiddel er til stede. Det økte medikamentopptaket har vært tilskrevet dannelsen av transiente porøsiteter i cellemembranen, noe som kan medvirke til transmembran transport av medikamenter inn i cellen. Den forbigående permeabilisasjon (åpning av hull i membranen) og etterfølgende spontan forsegling av cellemembranen kalles sonoporasjon.
Ultralyd har vært brukt for eksperimentell levering av terapeutiske midler, inkludert genetisk materiale, protein og kjemoterapeutiske midler blandet med eller innkapslet i mikroboblene. Ultralyd eksponering av disse mikroboblene når de befinner seg i den ønskede regionen gir målrettet levering av legemiddel til spesifikke anatomiske områder eller svulster. Vår forskningsgruppe har vist at lipid-innkapslede mikrobobler kan penetrere inn i celler ved lave, diagnostisk- akustiske innstillinger. Kombinasjonen av ultralyd, kontrastmidler og terapeutiske stoffer kan lede til en enkel, presis og økonomisk metode for å øke medikamentopptaket til f.eks. en kreftsvulst, ved hjelp av konvensjonelle ekko maskiner. Derfor ville en kombinasjon av et kjemoterapeutikum med et eksisterende ultralydkontrastmiddel være en plausibel måte for fremgang i f. eks. kreftbehandling.
Til tross for dagens brede spekter av behandlingstilbud, er kreft fortsatt en sykdom med økende forekomst og utbredelse over hele verden. Et problem i vellykket behandling eller kontroll av ondartede svulster er at de diagnostiseres sent i forløpet, ofte på et tidspunkt da de er lokalt avanserte eller allerede har metastasert. En slik tumor er da ikke kurativt operabel. Dette gjelder spesielt for kreft i bukspyttkjertelen, som er årsaken til dødsfall hos 600-650 pasienter i Norge årlig. Adenokarsinom i bukspyttkjertelen er fortsatt en av de mest dødelige kreftformene hos mennesker, og forekomsten og dødeligheten har vært stabil de siste fire tiårene.
Førti prosent av kreft i bukspyttkjertelen er lokal avanserte svulster, som ofte omfatter lokale store blodkar. Ca. 40 % av pasientene presenterer disseminerte svulster med tilstedeværelse av metastaser. Disse tumorer anses inoperable. Da kun 20 % av pasientene er operable så er oddsene for helbredelse av kreft i bukspyttkjertelen ganske små.
Kjemoterapi produserer objektiv respons, men er ikke kurativ, hovedsakelig fordi bruken av en effektiv dosering er sterkt hemmet av toksiske effekter i vitale organer. Det kan være at den desmoplastiske reaksjon indusert i denne type sykdom vanskeliggjør effektiv levering og penetrering av medikamenter til kreftceller. Som et resultat, er det meget lav overlevelse. Dødeligheten hos ikke-opererte pasienter er 50% innen 3 måneder, og 90% innen 12 måneder. Pyrimidin-analogen gemcitabin er den mest effektive monoterapi ved behandling og lindring av inoperabel kreft. Gemcitabin er et svært effektivt anti-tumor medikament, men dets toksiske virkninger begrenser den maksimale dose som kan administreres. Således er dets anvendelse i høydose kjemoterapiprotokoller, som er nødvendige for behandling av adenokarsinom, hemmet. Gemcitabin har blitt rapportert å forbedre kliniske symptomer og forlenge overlevelse med omlag en måned.
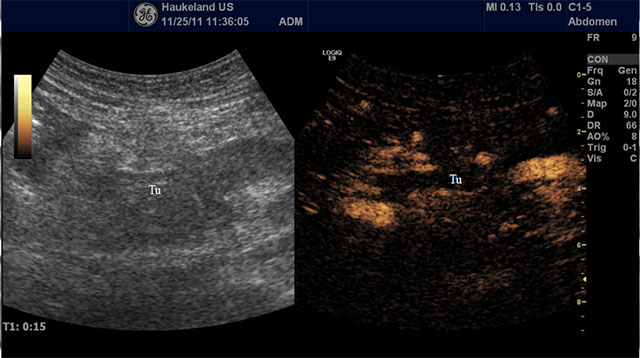
Figur 1. Adenocarcinom i pancreas. Bildet til venstre viser stor hypoekkogen tumor (Tu) i caput pancreatis med utløpere til omkringliggende vev. Bildet til hø.: Kontrastforsterket ultralyd viser en typisk hypovaskulær lesjon uten klare marginer. Bildene er fra en pasient som gjennomgår ultralyd sonoporasjon i kombinasjon med gemcitabin. Rundt tumor ses hypervaskulært omkringliggende pankreasvev.
Der er derfor nødvendig å utvikle terapeutiske verktøy basert på nye metoder som f.eks. ultralydrettet mikroboble-basert behandling for å øke det terapeutiske medikamentopptaket i svulster.
Vi har kombinert gemcitabin med et eksisterende kontrastmiddel (SonoVue) for å øke opptak og dermed forbedre effekten av kjemoterapibehandlingen. Studien er en åpen evalueringsstudie for denne type kombinasjonsbehandling av pasienter med inoperabel adeno-karsinom i bukspyttkjertelen. Prinsippet er basert på samtidig infusjon, dvs. blanding av gemcitabin og kontrastbobler, samt ultralyd-potensert levering av legemidler.
Pasienter med inoperabel kreft i bukspyttkjertelen, som har meldt seg frivillig til å delta og oppfylle inklusjonskriteriene, inkluderes. Nasjonale retningslinjer mhp., diagnostikk og behandling av disse pasienter følges. Vår mål er å forbedre eksisterende førstelinjebehandling ved å legge til ultralyd-veiledet og tidsstyrt sonoporasjon, målrettet på tumor.
Standard behandling av duktalt adenokarsinom er gemcitabin 1000 mg/m2 gitt som en 30 minutters intravenøs infusjon. Ved maksimal gemcitabin konsentrasjon i blodet, dvs. umiddelbart etter infusjon, tilsettes 4,8 ml SonoVue i små bolusdoser. Her etter sonoporeres målet (tumor) i 30 minutter. Behandlingen følger standard Gemzar protokoll med syv sykluser en gang i uken, etterfulgt av en ukes opphold, med mindre uakseptabel toksisitet oppstår. Påfølgende sykluser er en gang i uka i 3 sammenhengende uker ut av hver 4. uke. Alle behandlinger gjennomføres på poliklinisk basis.
Preliminære resultater virker lovende. De pasienter som har fått den kombinerte behandling har alle i snitt hatt flere behandlingssykluser som utrykk for vedvarende klinisk effekt av gitt behandling, sammenliknet med historiske data fra tidligere pasienter på Haukeland Universitetssykehus, behandlet med Gemzar. Redusert tumorstørrelse er også registrert. Ingen uønsket toksisitet eller andre uventede bivirkninger er registrert hittil. Etter fullførte 10 pasienter, kan det primære utfallet bli evaluert, og komplette data, inkludert sikkerhet og pasientens toleransedata kan presenteres.
Referanser
Sonoporation at a low mechanical index. A. Delalande, S. Kotopoulis, T. Rovers, C. Pichon, M. Postema. Bubble science, Engineering and Technology 01/2011 • Ultrasound-directed drug delivery. Postema M, Gilja OH. Curr Pharm Biotechnol. 2007 Dec;8(6):355-61. • Contrast-enhanced and targeted ultrasound. Postema M, Gilja OH. World J Gastroenterol. 2011 Jan 7;17(1):28-41. doi: 10.3748/wjg.v17.i1.28. • Sonoporation-Enhanced Chemotherapy Significantly Reduces Primary Tumour Burden in an Orthotopic Pancreatic Cancer Xenograft. Spiros Kotopoulis, Anthony Delalande, Mihaela Popa, Veronika Mamaeva, Georg Dimcevski, Odd Helge Gilja, Michiel Postema, Bjørn Tore Gjertsen, Emmet McCormack. Mol Imaging Biol. 2013 Jul 23. PMID: 23877869 • Treatment of human pancreatic cancer using combined ultrasound, microbubbles and gemcitabine: a clinical case study. Kotopoulis S, Dimcevski G, Gilja OH, Hoem D, Postema M. Med Phys. 2013 Jul;40(7):072902.