Av Roald Flesland Havre og Lars Birger Nesje. Medisinsk avdeling, Haukeland Universitetssykehus, Bergen
Som et tillegg til vanlig endoskopisk ultrasonografi (EUS) kan man benytte elastografi til nærmere karakteristikk av pankreassvulster. Elastografi er avbildning av elastiske vevsegenskaper fremstilt som ulike vevsområders relative hardhet. Per i dag er den endoskopiske elastografimetoden basert på registrering av vevsdeformasjon (strain) som skapes av vevsbevegelser fra aorta, hjerte eller respirasjon.
Operativitetsvurdering
Svulster i pankreas er ofte ondartede og har en dårlig prognose [1] fordi de på diagnosetidspunktet har metastasert eller vokst inn i ikke reseserbare kar og dermed må klassifiseres som lokalavanserte. Operable svulster, bortsett fra noen som gir tidlig gallestase og icterus, oppdages ofte nokså tilfeldig før de gir symptomer. Pga. økende bruk av CT og MRI påvises flere små fokale lesjoner i pankreas, både cystiske og solide [2]. Flere av disse blir henvist for nærmere morfologisk beskrivelse med EUS.
Elastografi fremstiller relativ vevshardhet kvalitativt ved hjelp av et fargekart. Dette fargekartet angir grad av deformasjon i vev som utsettes for en viss kompresjonskraft. Avbildningen presenteres i sann tid i et eget bilde der elastogrammet legges over det tilsvarende ultralydbildet (Fig 1). Metoden er kan registrere små endringer i posisjonen av ekkogene billedelementer i den aksiale retning (langs ultralydens stråleretning). Metoden baserer seg på endogen vevsbevegelse, dvs. aortapuls og cardiale bevegelser som overføres til pankreasvevet. Metoden kalles og kvasi-statisk elastografi, fordi den utnytter relativt sakte vevsbevegelser i forhold til det tidsintervall den evaluerer deformasjonen over. Metoden egner seg for karakteristikk av fokale pankreaslesjoner ved EUS der lesjonen kan fremstilles i nærfeltet, ca 1-4 cm fra ultralydproben.

Fig 1: Endoskopisk ultralyd av en jevnt hypoekkisk lesjon i pankreas, ca 18 mm i diameter til høyre. Til venstre samme bilde med et elastogram over. Tumor fremstår med hardere vev (blått) svarende til den hypoekkoiske lesjonen. Strain ratio mellom referansevev, B og tumorvev, A markert i B-mode bildet viste SR: 44.5. Histologi viste: ductalt adenokarsinom.
Det har vært lansert flere fremgangsmåter for å kvantifisere forskjeller i elastografi, blant annet beregning av deformasjonsgrad i prosent av utgangspunktet (strain, %) [3], sammenlikning av strain i to områder i bildet (strain ratio) [3-5]og bruk av gjennomsnittlig farge i aktuelle lesjon ved hjelp av en nummerert fargeskala fra 0-256[6]. Flere av disse metodene er arbeidskrevende og må gjøres som etterbehandling i egne dataprogrammer. Det gjør dem mindre egnet til klinisk anvendelse, men fungerer som valideringsvertøy for metoden. Generelt er det elastografibildet av en mer dynamisk natur enn det vanlige B-modebildet skapt med ultralyd (UL). Avhengig av om det foregår en kompresjon, dekompresjon eller man er mellom disse fasene vil bildet endre seg i sanntidspresentasjonen. Dette kan være bakgrunnen for at metoden har vist relativt store intra og interobservatør variasjoner [7]. Det er derfor viktig at vevsområdet lar seg komprimere mer eller mindre repeterende for å oppnå et reproduserbart elastografibilde, og man bør sammenligne avbildningene i same fase av kompresjon eller dekompresjon. Deformasjonen i den valgte ”region of interest” (ROI) kan fremstilles i form av en kurve på skjermen og gir umiddelbar tilbakemelding om kompresjonen er tilfredsstillende.

Fig 2: EUS-elastogram av en velavgrenset oval pankreastumor. På B-mode bildet til høyre fremstår lesjonen hyperekkoisk med tre små forkalkninger i randsonen, ikke typisk for ondartet svulst. Det er vanskelig å avgrense lesjonen mot omliggende pankreasvev på B-mode bildet til høyre, men dette fremstår tydeligere ved elastografi som fremstiller lesjonen homogent hardere enn omliggende pankreasvev. EUS-FNA: Tette epiteliale cellegrupper uten tegn til atypi. Oppfølging har vist at det ikke er en malign tumor.
Valideringstudier
Det har vært gjennomført flere multisenterstudier med EUS-elastografi. Den europeiske multisenterstudien (n=285) benyttet først en analyse av gjennomsnittlig farge i svulstene og definerte en cut-off på 175 av 256 for å skille mellom maligne og benigne svulster og fant sensitivitet 93.4, spesifisitet 66.0% og ROC-AUC: 0.89 [8]. Det samme materialet ble benyttet i en ”neural-network” analyse med avansert automatisert farge- og mønstergjenkjenning. Man oppnådde da sens. 87.6 og spes. 82.9 med ROC-AUC: 0.94 [9]. Vi har og brukt ulike evalueringsmetoder av vevshardhet i 43 pankreassvulster av ukjent etiologi. I vårt materiale var det færre maligne svulster 17(40%) enn i flere av de tidligere publiserte studiene. Vi benyttet en visuell analog skåring av vevshardhet fra 0-100, median strain ratio og en kategorisk visuell skala. Maligne nevroendokrine svulster (NET) og adenokarsinomer hadde signifikant høyere vevshardhet enn fokale pankreatitter, benigne NET og andre benigne lesjoner. Det var ikke signifikante forskjeller mellom de benigne lesjonene. Den kategoriske visuelle skåringen kunne ikke skille maligne fra benigne lesjoner med rimelig sikkerhet, men når grønne og røde farger dominerte, indikerte dette at lesjonen var godartet [10]. I likhet med andre studier har vi avbildet godartede tumores med EUS elastografi som fremstår som hardere enn referansevev (Fig 2), eksempler på dette er microcystiske/oligocystiske serøse adenomer og autoimmun pankreatitt (Fig 3).
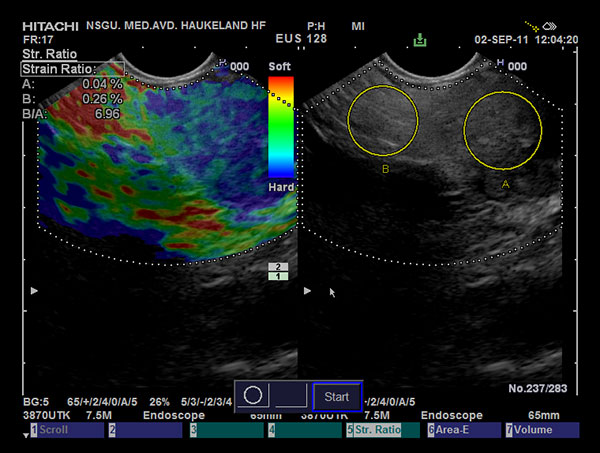
Fig 3: B-mode EUS (til høyre) viser en oppfylning i pankreas på ca 35 mm. i diameter. I elastogrammet fremstår denne med en klart hardere struktur enn omliggende pankreasvev. Strain ratio er beregnet mellom strain i referansevev, B dividert med strain i tumorvev, A markert på B-mode bildet. Strain ratio her er 6,96. EUS-FNA viste: reaktivt pregede celler uten typiske autoimmune forandringer. CT: autoimmun pankreatitt, oppfølging har bekreftet diagnosen.
Begrensninger
Noe av begrensningen ved EUS-basert elastografi av pankreaslesjoner er bruken av endogen vevsbevegelse som stresskilde. Individuelle forhold knyttet til dette vil påvirke deformasjonskraften og gi store individuelle variasjoner. Avhenging av retningen på deformasjonskraftene vil ulike områder i pankreas bli utsatt for ulik deformasjon, og en sammenlikning av strain i to ulike områder av billedplanet vil derfor ikke nødvendigvis ha forutsetninger for å vise den reelle forskjell i vevshardhet. Dette er viktig å kjenne til når man utfører EUS-elastografi av pankreas. Det gir seg utslag i at større lesjoner med diameter > 4 cm eller lesjoner som ligger dypt i forhold til ultralydproben, ikke gir gode nok elastografibilder hos enkelte pasienter. Elastografi avbilder sannsynligvis summen av flere fysiologiske prosesser som kan bidra til økt vevshardhet. En av disse er økt fibrose som man vet opptrer i mange maligne svulster gjennom en desmoplastisk reaksjon. Likeledes kan økt fibrose være et resultat av kronisk betennelse. Ødem med økt lokalt vevstrykk kan oppstå både ved akutte inflammatoriske prosesser og ved maligne svulster. I en studie på resesert tarmvev kunne vi ikke vise forskjell mellom vevshardhet i adenokarsinomer og i reseserte Mb. Crohn-lesjoner[11].
Kombinerte metoder i EUS
En kombinasjon av ulike endoskopiske ultralydmodaliteter kan gi mer detaljert avbildning av fokale pankreaslesjoner og således en mer treffsikker, non-invasiv eller minimal-invasiv vurdering av fokale solide pankreaslesjoner. Etter at en lesjon er sett på CT eller MRI, bør en CT utført etter pankreasprotokoll vurderes. Videre kan en god EUS med høyfrekvent UL som basis, suppleres med fargedoppleravbildning, som gir informasjon om karforsyningen i og omkring lesjonen, samt elastografi som kan fortelle hvorvidt lesjonen fremstår som reproduserbart hardere enn omliggende pankreas og fettvev. Kontrastforsterket UL kan fremstille perfusjonen (kapillærgjennomblødningen) og om lesjonen tømmes for en bolus av kontrast fortere enn omliggende pankreasvev. Til slutt kan man gjøre en nålebiopsi (EUS-FNA) dersom de foregående billedundersøkelsene ikke har gitt en sikker eller svært sannsynlig diagnose. Alle disse trinn kan utføres i en og samme EUS undersøkelse.
Vevshardhet kan beregnes på ulike metoder
Per i dag finnes det flere metoder for elastisitetsavbildning. I tillegg til den beskrevne metode som er tilgjengelig for EUS-applikasjonen, utnytter andre metoder måling av skjærekrefters hastighet som basis for å beregne lokal vevshardhet. Disse metodene omtales som ”shear-wave elastography” (SWE) [12-14], ”Acoustic radiation force impulse imaging” (ARFI) [15-17] eller ”transient elastography”[18-20]. Disse metodene har spesielle prober som kan avlevere en akustisk eller fysisk eksitasjonspuls i vevet, for deretter å måle skjærekreftenes hastighet. En fordel med disse metodene er at de gir et kvantitativt estimat for vevshardhet. Innenfor gastroenterologi er denne teknologien mest benyttet til å måle vevshardhet non-invasivt i lever ved utvikling av kronisk leversykdom, noe som kan redusere behovet for leverbiopsier [19,21-23]. Metodene har også egenskaper som kan gjøre elastisitetsberegninger mindre variable dersom de blir tilgjengelige for en endoskopisk applikasjon.
Konklusjon
EUS-basert elastografi er fortsatt en metode under utvikling. Dersom metoden skal bli klinisk nyttig i vurderingen av fokale pankreaslesjoner, må den kunne vurderes visuelt i løpet av EUS-undersøkelsen og eventuelt inneholde noen få og enkle målinger. Fremstillingen må være reproduserbar, og variasjonen mellom ulike tumortyper må gjenspeile trekk som ikke fremstilles tilsvarende godt ved andre billedmodaliteter. Elastografi er i vår praksis i dag nyttig som en tilleggsparameter ved EUS sammen med Doppleravbildning. Vi har også forventninger til at kontrastforsterket perfusjonsmåling blir en nyttig EUS-basert avbildningsmetode ved vurdering av fokale pankreaslesjoner [24,25].
Referanser
- http://www.kreftregisteret.no/no/Registrene/Kreftstatistikk/. In: Department NH ed, Kreftstatistikk. Oslo: Norwegian cancer registry; 2011
- Laffan TA, Horton KM, Klein AP, et al. Prevalence of unsuspected pancreatic cysts on MDCT. AJR Am J Roentgenol 2008;191:802-807
- Iglesias Garcia J, Larino Noia J, Abdulkader I, Forteza J, Dominguez-Munoz JE. Quantitative endoscopic ultrasound elastography: an accurate method for the differentiation of solid pancreatic masses. Gastroenterology 2010;139:1172-1180
- Dawwas MF, Taha H, Leeds JS, Nayar MK, Oppong KW. Diagnostic accuracy of quantitative EUS elastography for discriminating malignant from benign solid pancreatic masses: a prospective, single-center study. Gastrointest Endosc 2012
- Itokawa F, Itoi T, Sofuni A, et al. EUS elastography combined with the strain ratio of tissue elasticity for diagnosis of solid pancreatic masses. J Gastroenterol 2011;46:843-853
- Saftoiu A, Gheonea DI, Ciurea T. Hue histogram analysis of real-time elastography images for noninvasive assessment of liver fibrosis. AJR Am J Roentgenol 2007;189:W232-233
- Havre RF, Elde E, Gilja OH, et al. Freehand real-time elastography: impact of scanning parameters on image quality and in vitro intra- and interobserver validations. Ultrasound Med Biol 2008;34:1638-1650
- Saftoiu A, Vilmann P, Gorunescu F, et al. Accuracy of endoscopic ultrasound elastography used for differential diagnosis of focal pancreatic masses: a multicenter study. Endoscopy 2011;43:596-603
- Saftoiu A, Vilmann P, Gorunescu F, et al. Efficacy of an artificial neural network-based approach to endoscopic ultrasound elastography in diagnosis of focal pancreatic masses. Clin Gastroenterol Hepatol 2012;10:84-90 e81
- Havre R, Ødegaard S, Gilja OH, Nesje LB. Quantification of elastography in pancreatic focal lesions using endoscopic ultrasonography. In, Endoscopy. Stockholm, Sweden: Georg Thieme Verlag KG, Stuttgart; 2011:Abstract 1056
- Havre R, Waage JE, Leh S, et al. Strain assessment in surgically resected inflammatory and neoplastic bowel lesions. Ultraschall in Med 2012;Accepted
- Bercoff J, Tanter M, Fink M. Supersonic shear imaging: a new technique for soft tissue elasticity mapping. IEEE Trans Ultrason Ferroelectr Freq Control 2004;51:396-409
- Deffieux T, Montaldo G, Tanter M, Fink M. Shear wave spectroscopy for in vivo quantification of human soft tissues visco-elasticity. IEEE Trans Med Imaging 2009;28:313-322
- Gennisson JL, Muller M, Deffieux T, Tanter M, Fink M. Quantitative Viscoelasticity Mapping of Human Liver Using Supersonic Shear Imaging: Preliminary in Vivo Feasability Study. Ultrasound in Medicine and Biology 2009;35:219-229
- D’Onofrio M, Gallotti A, Mucelli R. Tissue quantification with acoustic radiation force impulse imaging: Measurement repeatability and normal values in the healthy liver. Am J Roentgenol 2010;1:132-136
- Gallotti A, D’Onofrio M, Pozzi Mucelli R. Acoustic Radiation Force Impulse (ARFI) technique in ultrasound with Virtual Touch tissue quantification of the upper abdomen. Radiol Med 2010;115:889-897
- Palmeri ML, Frinkley KD, Zhai L, et al. Acoustic radiation force impulse (ARFI) imaging of the gastrointestinal tract. Ultrason Imaging 2005;27:75-88
- Foucher J, Chanteloup E, Vergniol J, et al. Diagnosis of cirrhosis by transient elastography (FibroScan): a prospective study. Gut 2006;55:403-408
- Fraquelli M, Rigamonti C, Casazza G, et al. Reproducibility of transient elastography in the evaluation of liver fibrosis in patients with chronic liver disease. Gut 2007;56:968-973
- Sandrin L, Tanter M, Gennisson JL, Catheline S, Fink M. Shear elasticity probe for soft tissues with 1-D transient elastography. IEEE Trans Ultrason Ferroelectr Freq Control 2002;49:436-446
- Palmeri ML, Wang MH, Rouze NC, et al. Noninvasive evaluation of hepatic fibrosis using acoustic radiation force-based shear stiffness in patients with nonalcoholic fatty liver disease. J Hepatol 2011;55:666-672
- Bavu E, Gennisson JL, Couade M, et al. Noninvasive in vivo liver fibrosis evaluation using supersonic shear imaging: a clinical study on 113 hepatitis C virus patients. Ultrasound Med Biol 2011;37:1361-1373
- Rockey DC. Noninvasive assessment of liver fibrosis and portal hypertension with transient elastography. Gastroenterology 2008;134:8-14
- Dietrich CF, Ignee A, Braden B, et al. Improved differentiation of pancreatic tumors using contrast-enhanced endoscopic ultrasound. Clin Gastroenterol Hepatol 2008;6:590-597 e591
- Serra C, Felicani C, Mazzotta E, et al. Contrast-enhanced ultrasound in the differential diagnosis of exocrine versus neuroendocrine pancreatic tumors. Pancreas 2013;42:871-877