Introduksjon
Leverfibrose oppstår når øket mengde matriks proteiner akkumuleres ekstracellulært i levervev rammet av en kronisk inflammatorisk prosess. Fibrose kan utvikle seg ved de fleste kroniske leversykdommer uavhengig av etiologi, og kan progrediere til levercirrhose.
Korrekt vurdering av leverfibrose gir viktig diagnostisk og prognostisk informasjon. Selv om leverbiopsi fortsatt er betraktet som ”gullstandard” for vurdering av leverfibrose, har metoden flere begrensninger. For det første er dette en invasiv prosedyre med en vis risiko for komplikasjoner. Dessuten utgjør variasjoner i den intrahepatiske sykdommsutbredelse (sampling error) en ikke ubetydelig feilkilde. Vesentlig er det også intra-/interobserver variabilitet (1,2). Nyere forskning tyder på at til og med avansert leverfibrose kan være reversibel og kan forsvinne spontant etter vellykket behandling av grunnleggende sykdom. For å dokumentere slike dynamiske forandringer ved leverfibrose har det vært behov for nye sensitive, enkle og ikke invasive diagnostiske metoder. Forskning på dette felt har de siste årene resultert i uvikling av ikke invasive markører av leverfibrose med forskjellig sensitivitet og spesifisitet. Det nyeste bidraget til de ikke invasive metodene er transient elastografi (Fig.1., FibroScan, Echosens, France).
Biokjemiske markører
Slike markører bør være enkele, raske, reproduserbare og sensitive. Metodologisk har man anvendt både direkte og indirekte markører for fibrose. Direkte markører undersøker metabolismen av leverens ekstracellulære matriks direkte. Til denne gruppen tilhører: kollagener (prokollagen I og III, type IV kollagen ), hyaluron syre, laminin, YKL-40, kollagenaser og deres hemmere og TGF-b. Klinisk bruk av disse markørene er begrenset grunnet deres utslag i aktiv eller ko-eksisterende inflammasjon (3,4,5,6,7) . Indirekte markører av leverfibrose reflekterer forandringer i leverens funksjon og i ekstracellulært matrix indirekte. For eksempel er ASAT/ALAT ratio (AAR) en enkel og klinisk lett anvendelig markør. AAR øker hos pasienter som progredierer fra kronisk hepatitt til levercirrhose.
AAR >1 har tidligere vært vist av både oss og andre å predikere avansert fibrose, cirrhose og cirrhose relatert mortalitet (8,9). ASAT/platelet ratio index (APRI) ble vist klinisk anvendelig i diagnostikk av signifikant fibrose og cirrhose ved kronisk hepatitt C (CHC) (10). Mer komplisert Forns’ index (7.811 − 3.131 ln (platelet-count) + 0.781 ln (gGT) + 3.467 ln (age) − 0.014 (cholesterol) har vist diagnostisk verdi i differensiering mellom ingen/minimal fibrose og signifikant fibrose hos pasienter med CHC men gir ikke noe informasjon om cirrhose (11). Den hittil mest klinisk vurderte testen, FibroTest, inkluderer gGT , bilirubin, haptoglobin, apolipoprotein A1 og a2-makroglobulin, korrigert for alder og kjønn (12). I en nylig studie ble FibroTest sammenliknet med APRI og Forns’ index hos 190 pasienter med CHC. FibroTest viste da høyeste presisjon i vurdering av signifikant fibrose og cirrhose (13).
Transient Elastografi
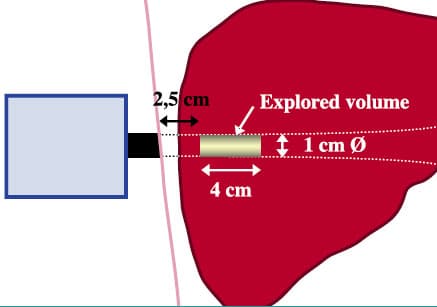
FibroScan er en spesielt designet enhet som består av en probe, komputer med tilpasset programvare og kontrollenhet (14 og Fig.1.). Proben inneholder en mekanisk bølgegenerator og en ultralyd enhet. Generator produserer en mekanisk impuls i form av en lavfrekvent elastisk bølge mot hudoverflaten som videre beveger seg gjennom leveren (Fig.2). Bevegelse av den elastiske bølgen blir monitorert av probens ultralyddel. Bølgens hastighet er proporsjonal med leverens stivhet; jo høyre bølgens hastighet jo stivere leverens vev. Denne teknikken gjør det mulig å estimere leverens elastisitet. Resultat angis i kilopascal (kPa). Leverens stivhets målinger (LSM) varierer fra 2.5 til 75 kPa (Fig.3).

Figur 3. Klinisk betydning av LSM cut-off’s i kronisk leversykdom. Når LSM er mellom 2.5 og 7 kPa, er mild eller ingen fibrose mest sannsynlig, mens når LSM er over 12.5 kPa, er cirrhose mest sannsynlig (fra Laurent C. J Hepatol 2008;48:835-847).
Undersøkelsen er lett å gjennomføre, unntatt hos pasienter med fedme, og tar ca. 10 min. I en nylig studie (15) var LSM sammenliknet med histologisk METAVIR fibrose (F0 til F4) hos 251 pasienter med CHC. LSM korrelerte godt med histologisk grad av fibrose. De optimale cutoff verdier for F>/=2 og F4 var henholdsvis 8.8 og 14.6 kPa. Sammenliknet med AAR og APRI i en annen studie var LSM best i diagnostisering av signifikant fibrose og cirrhose. Nye studier viser korrelasjon av LSM med andre kliniske parametere som portvenetrykk og øsofagus varicer av ulik grad.
Konklusjon
For å redusere antall leverbiopsier har vi behov for nye ikke invasive metoder for vurdering av leverfibrose og cirrhose. Selv om mange nye ikke invasive markører har blitt studert de siste årene, er deres klinisk anvendelse foreløpig begrenset. LSM er lett og rask å anvende klinisk med god reproduserbarhet og ser ut til å ha større klinisk verdi enn biokjemiske markører. Nye studier vil endelig etablere LSM’s klinisk anvendelse. Vi tokk FibroScan i klinisk bruk på Aker Universitetssykehus i mai 2007. Hittil har vi gjennomført ca. 400 undersøkelser hos pasienter med ulike leversykdommer.
Referanser
- Cadranel JF. at al. Hepatology. 2000;32:477-481
- Colloredo G. at al. J Hepatol. 2003;39:239-244
- Murawaki Y. at al. J Gastroenterol Hepatol 2001;16:777-781
- Guechot J. at al. Clin Chem. 1996;42:558-563
- McHutchison JG. at al. J Gastroenterol Hepatol 2000;15:945-951
- Saitou Y. at al., World J Gastroenterol 2005;11:476-481
- Boeker KH. at al. Clin Chim Acta 2002;316:71-81
- Haukeland JW, at al. Scand J Gastroenterol. 2008;2:1-8.
- Giannini E. at al. Arch Intern Med 2003;163:218-224
- Wai CT. at al. Hepatology. 2003;38:518-526
- Forns X. at al. Hepatology. 2002;36:986-992
- Imbert-Bismut F. at al. Lancet 2001;357:1069-1075
- Sebastiani G. at al. J Hepatol. 2006;44:686-693
- Sandrin L. at al. Ultrasound Med Biol 2003;29:1705-1713
- Ziol M. at al. Hepatology. 2005;41:48-54